食藥署今天(30日)公布,鴻汶醫藥實業有限公司生產的重鬱症用藥「鴻汶欣樂膠囊」30毫克與60毫克規格的產品,因溶離試驗結果未符合規格,業者主動啟動全面回收,總計回收69.3萬顆,同時暫停生產並予以重新研發。食藥署已要求業者於112年6月16日前完成回收作業,並提交成果報告書及後續預防措施。
▲ 食藥署已要求業者於112年6月16日前完成回收作業(圖/食藥署提供)
鴻汶欣樂膠囊的主成分為duloxetine hydrochloride,適應症為重鬱症、廣泛性焦慮症、糖尿病周邊神經痛和纖維肌痛等。食藥署副署長陳惠芳指出,同成份、同劑型但不同劑量的鴻汶欣樂膠囊屬於「延遲控釋膠囊」,需通過胃酸消化後,才能在腸道中發揮其療效。
陳惠芳進一步說明,該藥品效期為2年,在12個月安定性試驗中,發現溶離試驗結果未達標準。在模擬胃酸環境下,溶離度不應超過10%,但實際試驗結果在胃部就已超過10%溶離,可能影響腸胃吸收及藥效。因此,業者主動通報並展開回收,全面暫停生產後重新研發。
根據食藥署公布的數據,鴻汶欣樂膠囊30毫克需回收的批號為:BAT022、BBU103、BBW141、BAU076、BBO005、BBM085、BBS024、BAS006、BAS007、BBM086、BBO006、BBU104、BAT023、BAU077、BAQ071、BBW140、BAQ070、BBS025,共18批。
「”鴻汶”欣樂膠囊60毫克」則要回收:BBT053、BBV038、BAS004、BAT020、BBS020、BBS021、BBW137、BBS016、BBW136、BBO001、BBS022、BAX055、BBO003、BAQ072、BBS017、BAT021、BBV039、BAS009、BBV040、BAS008、BBV037、BAX057、BBS018、BBS023、BBT052、BAX054、BBW139、BBW138、BAU081、BAX056、BAT025、BAQ073、BAS005、BAT024、BBO002、BBT054、BBO004、BBS019、BBT055,共39批。

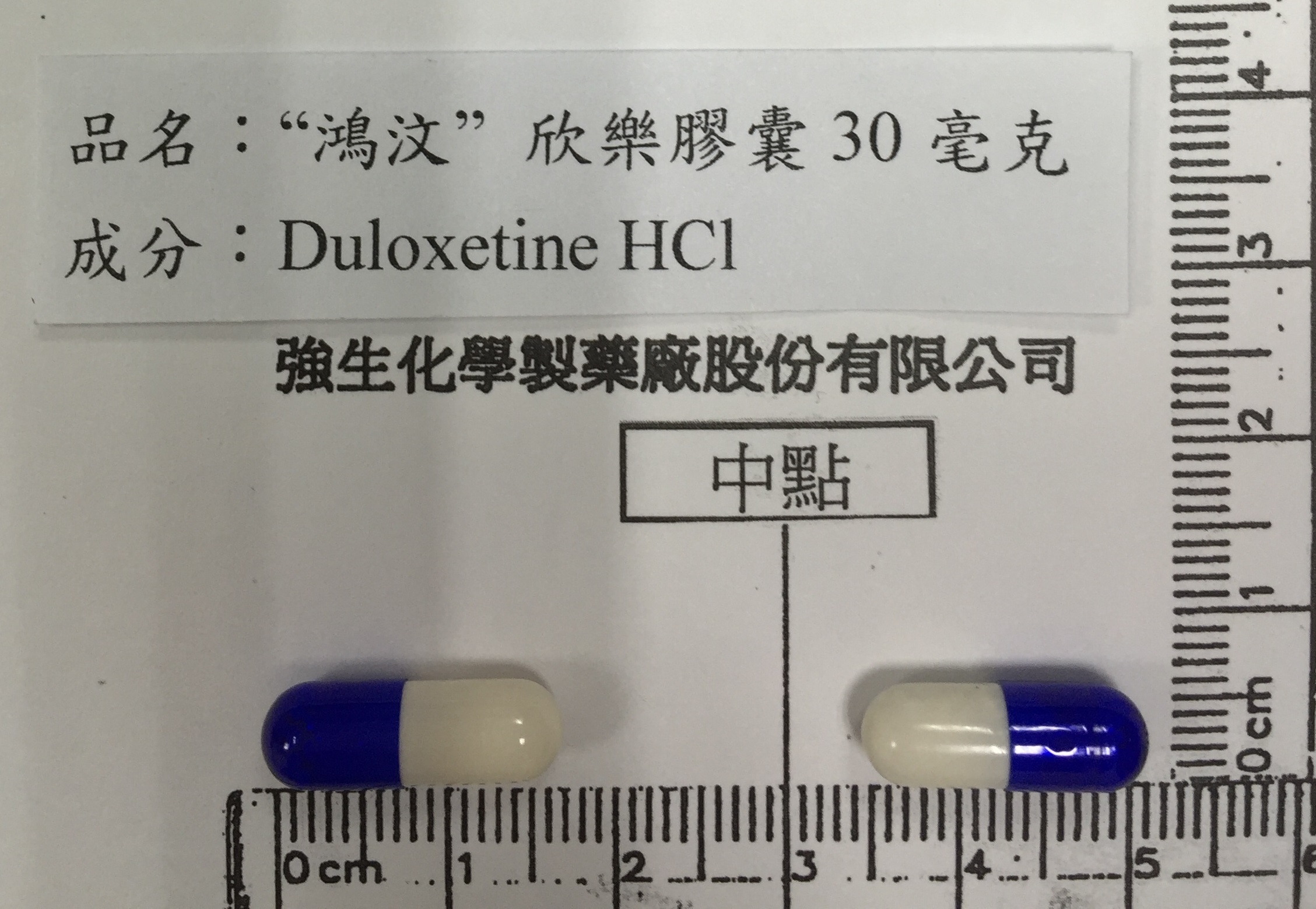
▲▼ 欣樂膠囊藥物外觀。(圖/食藥署提供)

食藥署呼籲,民眾如發現持有符合回收批號之藥品,請勿再使用,並與該公司連繫進行更換退貨。陳惠芳建議,持有患者如果因回收而需要更換藥品,可與醫生討論替代治療或改用其他品牌之同成份藥品。食藥署將持續關注該事件,並請業者提出改善計畫。
國內藥品回收事件屢見不鮮,食藥署應加強監管,保障民眾用藥安全。一旦發現藥品製程不合規格,業者應立即通報並回收,以降低對患者療效的影響。同時,患者及其家屬也應主動關注回收訊息,避免使用不合格藥品。未來,食藥署將進一步加強藥品品質監管,向業者多次抽驗,並要求業者詳細報告整改情況。希望在食藥署和業者的共同努力下,能夠確保藥品品質安全,降低民眾用藥風險。













留言評論